
Leki z grupy agonistów GLP-1 to nowość na rynku preparatów odchudzających. W mediach mówi się o nich w samych superlatywach, ale na ile są one tak naprawdę bezpieczne i skuteczne? Dlaczego większość osób zaprzestaje ich stosowania już po kilku miesiącach i czym grozi przerwanie leczenia? Co sprawia, że utrata wagi w pewnym momencie się zatrzymuje? Odpowiedzi na te i wiele innych pytań poznamy w tej serii 24 artykułów poświęconych lekom GLP-1.
W poprzednich artykułach omówiliśmy już korzyści, jakie niesie za sobą farmakologiczne zwiększanie aktywności GLP-1 w kontekście utraty wagi, względnie do spustoszenia, jakie sieje w organizmie otyłość. Poruszyliśmy również kwestię działań niepożądanych, w tym tych najbardziej powszechnych, takich jak reakcje ze strony układu pokarmowego, czy utrata masy mięśniowej, jak również tych, które występują rzadziej, takich jak rak tarczycy, zapalenie trzustki czy rak trzustki. Podsumowaliśmy także bilans zysków i strat, wskazując, u kogo korzyści ze stosowania tych leków mogą znacznie przewyższać ryzyko – przynajmniej w perspektywie krótkoterminowej.
A może istnieje sposób, by czerpać korzyści z działania GLP-1 bez skutków ubocznych? Czy aktywność tego hormonu można stymulować w sposób naturalny, poprzez odpowiednie zmiany w diecie i stylu życia [1]? Sprawdźmy, co na to badania naukowe.
Dieta i ruch: jak naturalnie pobudzić GLP-1?
Na początek: aktywność fizyczna. Ćwiczenia wydają się doraźnie zwiększać poziom GLP-1 w organizmie [2]. Przeprowadzono w tym zakresie pięć badań, z czego w czterech odnotowano wyższe stężenie GLP-1 po treningu interwałowym o wysokiej intensywności (HIIT) oraz sprinterskim treningu interwałowym (SIT), a także po treningu ciągłym o umiarkowanej intensywności (MICT) [3]. Co ciekawe, nie stwierdzono wyraźnych różnic między treningiem interwałowym a ciągłym o umiarkowanej intensywności [3].
W porównaniu z grupami kontrolnymi, w których badani nie ćwiczyli wcale, oba rodzaje aktywności fizycznej (zarówno interwały, jak i trening ciągły) wywoływały istotny wzrost stężenia GLP-1 bezpośrednio po wysiłku oraz 30 do 90 minut później [3]. Istnieje niestety podejrzenie stronniczości publikacji (ang. publication bias), co oznacza, że autorzy mogli celowo pominąć badania dla siebie niewygodne, zniekształcając tym samym ogólny obraz wyników [3].
Pamiętajmy jednak, że ruch to zdrowie, niezależnie od tego, jak wpływa na poziom GLP-1. Dowody naukowe nie pozostawiają wątpliwości: na zwiększeniu aktywności fizycznej skorzystać może niemal każdy [4].
A co z dietą? Wśród żywności, napojów i przypraw istnieje wiele produktów które, jak wykazano w badaniach, podnoszą poziom GLP-1 endogennego, czyli wytwarzanego wewnątrz organizmu [1]. Tylko czy ten naturalny GLP-1 może stanowić alternatywę dla leków naśladujących jego działanie, takich jak Ozempic [5]?
Aby w pełni zrozumieć to zagadnienie, warto wrócić do jednego z pierwszych artykułów w tej serii, pt. „Jad jaszczurki zmienia medycynę. Oto jak działa Ozempic”
Wyjaśniamy tam, czym GLP-1 tak właściwie jest i na czym dokładnie polega mechanizm jego działania. Poziom endogennego GLP-1 wzrasta i spada w odpowiedzi na spożywane posiłki [5]. Natomiast podczas przyjmowania leków naśladujących GLP-1 stężenie tego hormonu we krwi pozostaje stosunkowo stałe i wysokie [5], choć określenie „wysokie” jest tu sporym niedopowiedzeniem.
GLP-1 z leków vs. GLP-1 z diety: porównanie stężeń
Całkowite stężenie tych leków we krwi wynosi z reguły około 20–30 nanomoli/litr [6]. Dla porównania: po posiłku poziom GLP-1 w organizmie wzrasta o maksymalnie 20–30 pikomoli/litr (Wykres 1) [5].
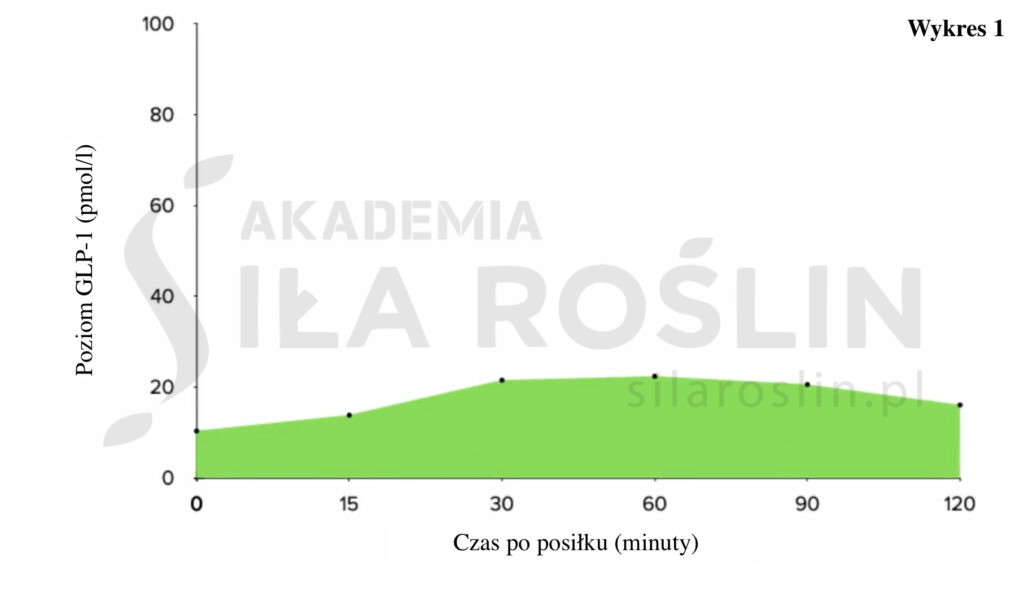 Przedrostek „nano-” oznacza jedną miliardową, a „piko-” jedną bilionową. Poziom leków jest więc około tysiąc razy wyższy (Wykres 2) [5]. Czy osiągnięcie takich wartości w sposób naturalny, poprzez zmiany w diecie, jest w ogóle możliwe?
Przedrostek „nano-” oznacza jedną miliardową, a „piko-” jedną bilionową. Poziom leków jest więc około tysiąc razy wyższy (Wykres 2) [5]. Czy osiągnięcie takich wartości w sposób naturalny, poprzez zmiany w diecie, jest w ogóle możliwe?
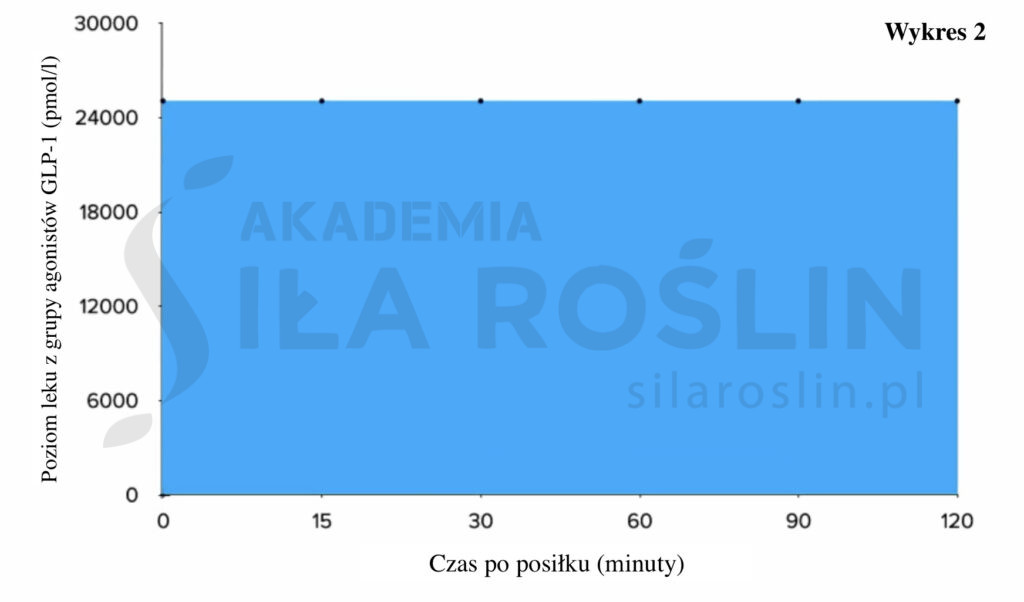 Część tej rozbieżności może wynikać z faktu, że do badań laboratoryjnych pobiera się krew żylną, a zanim endogenny GLP-1 dotrze do żył przebyć musi długą drogę [5]. Wydzielany jest w jelitach, następnie przechodzi przez wątrobę, serce i płuca, potem trafia do tętnic i dopiero na końcu do żył, skąd laborant pobiera próbkę [5]. Ponieważ naturalny GLP-1 jest szybko dezaktywowany przez enzym DPP-4, poziom tego hormonu we krwi żylnej jest niższy niż w krwi tętniczej, na którą wystawione są receptory GLP-1 w całym ciele [5]. Różnica ta jest jednak stosunkowo niewielka (10–30%) [5].
Część tej rozbieżności może wynikać z faktu, że do badań laboratoryjnych pobiera się krew żylną, a zanim endogenny GLP-1 dotrze do żył przebyć musi długą drogę [5]. Wydzielany jest w jelitach, następnie przechodzi przez wątrobę, serce i płuca, potem trafia do tętnic i dopiero na końcu do żył, skąd laborant pobiera próbkę [5]. Ponieważ naturalny GLP-1 jest szybko dezaktywowany przez enzym DPP-4, poziom tego hormonu we krwi żylnej jest niższy niż w krwi tętniczej, na którą wystawione są receptory GLP-1 w całym ciele [5]. Różnica ta jest jednak stosunkowo niewielka (10–30%) [5].
Jak to się dzieje, że leki naśladujące GLP-1 pozostają w organizmie tygodniami, a nie tylko przez kilka minut? Są one chemicznie zmodyfikowane tak, by przyłączać się do albuminy, czyli białka, które występuje w osoczu najobficiej [2]. Choć więc całkowity poziom leku we krwi mieści się w zakresie nanomolowym (15–40 nmol/l), duża jego część jest silnie związana z białkami [5]. Poziom wolnej substancji aktywnej (tej, która może faktycznie oddziaływać na receptory w tkankach) jest już około sto razy niższy, z wartościami w zakresie pikomolowym (180–350 pmol/l) (Wykres 3) [5].
 Zatem, choć na pierwszy rzut oka stężenie leku w osoczu wydaje się ekstremalnie wysokie, w rzeczywistości może być ono zbliżone do poziomu GLP-1 endogennego, możliwego do osiągnięcia dzięki silnej, żywieniowej stymulacji [5]. No dobrze, ale mówimy tu o wartościach rzędu 20–30 pmol/l vs. 180–350 pmol/l. Różnica jest więc trochę mniej szokująca, ale mimo wszystko wciąż spora.
Zatem, choć na pierwszy rzut oka stężenie leku w osoczu wydaje się ekstremalnie wysokie, w rzeczywistości może być ono zbliżone do poziomu GLP-1 endogennego, możliwego do osiągnięcia dzięki silnej, żywieniowej stymulacji [5]. No dobrze, ale mówimy tu o wartościach rzędu 20–30 pmol/l vs. 180–350 pmol/l. Różnica jest więc trochę mniej szokująca, ale mimo wszystko wciąż spora.
Za regulację spożycia pokarmu odpowiada GLP-1 w mózgu, jednak obecnie nie jest jasne, jak to się ma do poziomu tego hormonu we krwi [6]. Skoro głównym źródłem wydzielania GLP-1 są jelita, czy nie zostałby on rozłożony przez enzymy we krwi, zanim dotarłby w większej ilości do mózgu [7]? Hormon ten przekracza barierę krew-mózg, ale czy do mózgu dociera w wystarczającej ilości [8]? Jak się okazuje, GLP-1 jest produkowany również przez nerwy w samym pniu mózgu [8], a liczne dowody wskazują na to, że leki naśladujące GLP-1 hamują apetyt właśnie za pośrednictwem tych mózgowych receptorów [7]. Jak wobec tego klinicznie istotny wpływ mogą wywierać stężenia we krwi możliwe do osiągnięcia sposobami naturalnymi, dzięki diecie stymulującej jelitowe wydzielanie GLP-1 [5]?
Prawdą jest, że GLP-1 uwalniany z komórek jelitowych ulega szybkiej degradacji, co prowadzi do niskiego stężenia ogólnoustrojowego, ale działanie hormonu wydaje się być pośredniczone przez stymulację nerwu błędnego [5]. Nerw ten łączy jelita bezpośrednio z pniem mózgu – jest to więc „łącze bezpośrednie” z mózgiem, które nie musi polegać na transporcie przez krew.
Ale chwila, przecież receptory GLP-1 znajdują się także w trzustce, nerkach, wątrobie i sercu [9]. Po co organizm miałby umieszczać je w narządach obwodowych, skoro hormon działa głównie poprzez nerw błędny [5]? Możliwe, że silne bodźce (np. duży posiłek) potrafią podnieść poziom GLP-1 we krwi w stopniu na tyle znaczącym, że aktywują również te receptory obwodowe [5].
Możliwe zatem, że w normalnych okolicznościach mechanizm działania endogennego GLP-1 wygląda następująco: jemy posiłek, a GLP-1 wysyła sygnał hamujący apetyt bezpośrednio do mózgu, za pośrednictwem nerwu błędnego. Następnie mózg przekazuje te informacje do odpowiednich układów w całym organizmie [5]. Natomiast leki naśladujące GLP-1, po podaniu dożylnym, krążą we krwi i docierają bezpośrednio do wszystkich narządów, w tym do mózgu [5].
Można przypuszczać, że w obu tych mechanizmach działałby wyjątkowo silny bodziec żywieniowy stymulujący aktywność GLP-1, np. duży posiłek [5]. Czy GLP-1 w naturalnym stężeniu fizjologicznym naprawdę może hamować apetyt? Do ostatecznego rozstrzygnięcia tej kwestii potrzebujemy badań klinicznych z udziałem ludzi.
Co mówią badania kliniczne? Zaskakujące wyniki
Jedno z nich opublikowane zostało w 1999 r. Wykazano tutaj, że dożylne podanie różnych dawek GLP-1 skutkuje zależną od dawki redukcją głodu i spożycia pokarmu [10]. Tylko że skuteczne dawki stosowane w badaniach infuzyjnych podnosiły poziom GLP-1 we krwi co najmniej czterokrotnie, a żywność stymulująca produkcję GLP-1 zazwyczaj jedynie go podwajała [11]. Może wobec tego odnotowany w badaniu efekt nie jest możliwy do osiągnięcia bez udziału leków? Wlew z dużą dawką GLP-1 wyraźnie zmienił odczuwanie głodu i, co za tym idzie, zachowania żywieniowe, ale może sama stymulacja dietetyczna to w tym przypadku za mało [12]?
Jak już wcześniej wspomnieliśmy, jedzenie podnosi poziom GLP-1 we krwi tylko do około 20 pmol/l [12], ale jak się okazuje może to być wzrost w pełni wystarczający. Przytoczone badanie [10] pokazało, że znaczącą redukcję spożycia pokarmu (nawet o 30–35% w ramach posiłku typu „jesz, ile chcesz”) uzyskać można, podnosząc poziom GLP-1 zaledwie do 10, 15, czy nawet 5 pmol/l (Wykres 4).
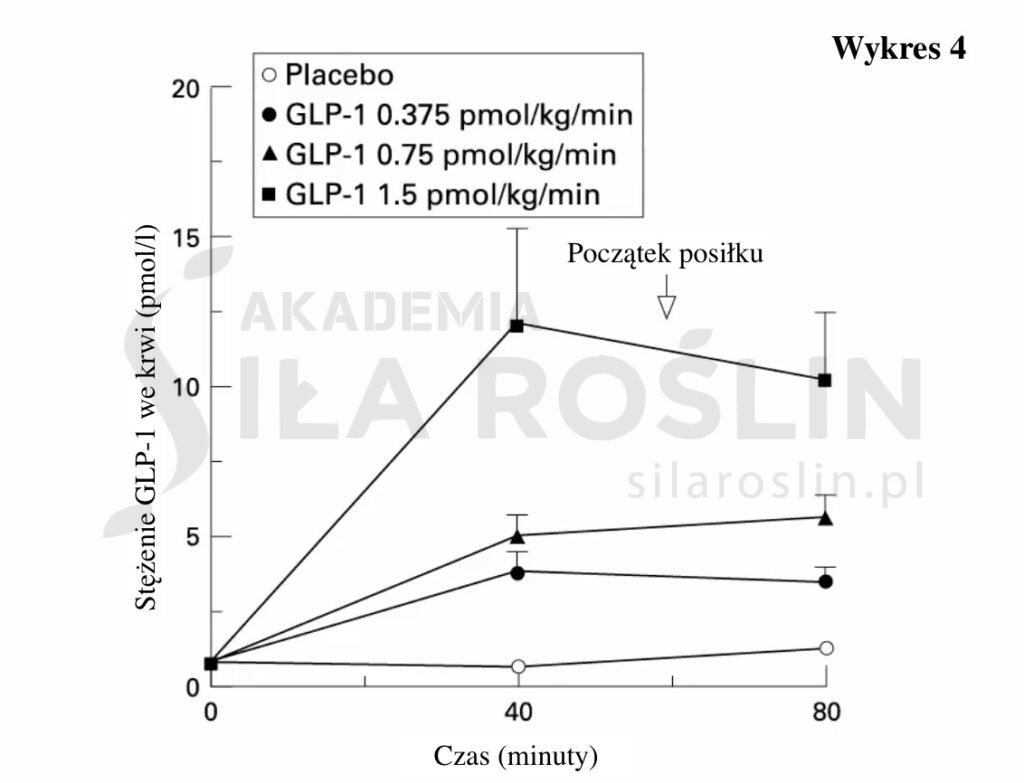 Są to wartości jak najbardziej osiągalne za pomocą diety. Zatem choć fizjologiczne stężenia GLP-1 (niskie z powodu szybkiej dezaktywacji przez enzym DPP-4) z pozoru mogą wydawać się nieskuteczne, już niewielki wzrost uzyskany dzięki stymulacji dietetycznej może mieć istotne znaczenie kliniczne [5]. Nie musimy więc dążyć do poziomów, jakie osiągnąć można tylko przy zastosowaniu leków [5]. Jeśli się nad tym zastanowić, jest to całkiem logiczne. W końcu po co organizm człowieka miałby, w odpowiedzi na jedzenie, produkować hormon hamujący apetyt, gdyby nie prowadziło to do faktycznego zahamowania apetytu?
Są to wartości jak najbardziej osiągalne za pomocą diety. Zatem choć fizjologiczne stężenia GLP-1 (niskie z powodu szybkiej dezaktywacji przez enzym DPP-4) z pozoru mogą wydawać się nieskuteczne, już niewielki wzrost uzyskany dzięki stymulacji dietetycznej może mieć istotne znaczenie kliniczne [5]. Nie musimy więc dążyć do poziomów, jakie osiągnąć można tylko przy zastosowaniu leków [5]. Jeśli się nad tym zastanowić, jest to całkiem logiczne. W końcu po co organizm człowieka miałby, w odpowiedzi na jedzenie, produkować hormon hamujący apetyt, gdyby nie prowadziło to do faktycznego zahamowania apetytu?
 Źródło: NutritionFacts.org
Źródło: NutritionFacts.org
Bibliografia:
[1] Boosting GLP-1 by Natural Products – PubMed
[2] Embracing the Pros and Cons of the New Weight Loss Medications (Semaglutide, Tirzepatide, Etc.) – PubMed
[3] Acute effect of high-intensity interval training versus moderate-intensity continuous training on appetite-regulating gut hormones in healthy adults: A systematic review and meta-analysis – PubMed
[4] Health Benefits of Physical Activity: A Strengths-Based Approach – PubMed
[5] Endogenous glucagon-like peptide (GLP)-1 as alternative for GLP-1 receptor agonists: Could this work and how? – PubMed
[6] Glucagon-like peptide-1: Are its roles as endogenous hormone and therapeutic wizard congruent? – PubMed
[7] Are GLP-1R agonists the long-sought-after panacea for obesity? – PubMed
[8] Effect of protein, fat, carbohydrate and fibre on gastrointestinal peptide release in humans – PubMed
[9] Glucagon-like peptide 1 (GLP-1) – PubMed
[10] Glucagon-like peptide-1: a potent regulator of food intake in humans – PubMed
[11] Use of satiety peptides in assessing the satiating capacity of foods – PubMed
[12] How Satiating Are the 'Satiety’ Peptides: A Problem of Pharmacology versus Physiology in the Development of Novel Foods for Regulation of Food Intake – PubMed
