Dieta naśladująca post w leczeniu łączonym z chemioterapią
Wstęp: Jakiś czas temu opublikowaliśmy dwa artykuły na temat ogólnej skuteczności chemioterapii (Czy chemioterapia jest tak naprawdę skuteczna?, W jakim stopniu chemioterapia przyczynia się do poprawy przeżywalności?). A co jeśli leczenie nowotworu uzupełnić dodatkowo postem? Jest to ostatni z serii czterech artykułów, w których postaramy się odpowiedzieć właśnie na to pytanie. Zapraszamy do lektury.
Wszystkie artykuły z tej serii:
- Post w leczeniu nowotworów: a co z kacheksją?
- Post w leczeniu łączonym z chemio- i radioterapią
- Post w leczeniu łączonym z chemioterapią ‒ co na to badania kliniczne?
- Dieta naśladująca post w leczeniu łączonym z chemioterapią
Krótkotrwałe odstawienie jedzenia w trakcie chemioterapii może stanowić pierwszy krok na drodze do rozwiązania odwiecznego problemu z większością metod leczenia nowotworów: jak zabić raka, nie zabijając przy tym pacjenta [1]. Krótkotrwały post, rozpoczęty na przykład 48 godzin przed chemioterapią i przerwany 24 godziny po jej zakończeniu, zmniejszając toksyczność leczenia, może łagodzić skutki uboczne chemioterapii [2]. Jak do tej pory nie przeprowadzono jednak żadnych badań nad postem w kontekście potencjalnego hamowania rozwoju raka, tj. wpływu na wzrost guza, ryzyko wystąpienia przerzutów, czy na rokowania choroby [3]. I niestety nic nie wskazuje na to, by coś miało się w tym obszarze zmienić [3]. Zatem rozpatrując kwestię: „Przed chemioterapią: pościć albo nie pościć?” [4], „należy podkreślić, że dowody pochodzące z badań z udziałem ludzi są w dalszym ciągu bardzo ograniczone” [4].
Według niektórych specjalistów skuteczność chemioterapii poprawiać może już samo złagodzenie skutków ubocznych [5]. Można bowiem założyć, że dzięki niemu pacjenci mogliby przyjmować większe dawki leków [5]. Przykładowo: leczniczy potencjał powszechnie stosowanych leków przeciwnowotworowych jest ograniczony przez związane z ich przyjmowaniem uszkodzenia serca i nerek [5]. Nie ma jednak pewności, czy zwiększenie maksymalnej tolerowanej dawki chemioterapii przełożyłoby się na poprawę przeżycia, czy jakości życia pacjentów [6]. Na razie cieszmy się z tego, że skutków ubocznych jest mniej, niezależnie od tego, czy wpływa to jakoś na skuteczność leczenia.
Niektórzy onkolodzy do postu podchodzą sceptycznie ze względu na ryzyko niedożywienia [7]. Obawa ta znajduje odzwierciedlenie w oficjalnych zaleceniach w zakresie żywienia pacjentów nowotworowych [8]. Dzień czy dwa głodówki może i nikomu by nie zaszkodziły [8]. Problem polega na tym, że pacjenci mogą chcieć te cykle postu stopniowo wydłużać [8]. W związku z powyższym, do czasu pojawienia się niezbitych dowodów na to, że takie leczenie łączone niesie za sobą jakieś rzeczywiste korzyści, post w czasie chemioterapii jest niezalecany [8].
Nawet zwolennicy postu przyznają, że pacjenci z poważną niedowagą, zanikiem mięśni, czy niedożywieniem nie są do tej metody leczenia dobrymi kandydatami, nawet w przypadku głodówki krótkotrwałej [2]. Jednak jak wynika z danych pozyskanych w wyniku obserwacji setek pacjentów, nic nie wskazuje na to, by krótkotrwały post, czy dieta naśladująca post, miały się wiązać z jakimikolwiek poważnymi działaniami niepożądanymi w zakresie niedożywienia czy utraty wagi [9]. Pacjenci, którzy w trakcie postu rzeczywiście schudli, z reguły odzyskiwali utracone kilogramy jeszcze przed kolejnym cyklem chemioterapii, a zmiany w masie ciała nie powodowały u nich żadnych zauważalnych szkód [10].
A nawet jeśli łączenie chemioterapii z postem miałoby być w jakimś stopniu ryzykowne, chodzi tu przecież o raka ‒ pewne ustępstwa są nieuniknione [9]. Pacjenci godzą się na leczenie ze świadomością ryzyka wystąpienia skutków ubocznych nie tylko poważnych, ale wręcz zagrażających życiu [9]. Może warto zaryzykować także w przypadku postu? W końcu złagodzenie choćby części skutków ubocznych chemioterapii może być tego warte.
Tymczasem przemysł farmaceutyczny próbuje już oczywiście odtworzyć dobroczynne działanie postu przy pomocy leków [11]. Prawdą jest, że leki naśladujące post mogą być dla pacjentów opcją wygodniejszą ‒ łatwiej jest przecież połknąć tabletkę niż odmawiać sobie przez jakiś czas jedzenia [11]. Problem polega na tym, że miną zapewne lata, zanim te leki pojawią się w ogóle na rynku [11]. Nie mówiąc już o tym, że mało prawdopodobne jest, by okazały się one równie skuteczne i bezpieczne co post [11]. A może efekty jak przy poście można uzyskać również dzięki odpowiednio dostosowanej diecie? Może całkowita głodówka nie jest wcale konieczna?
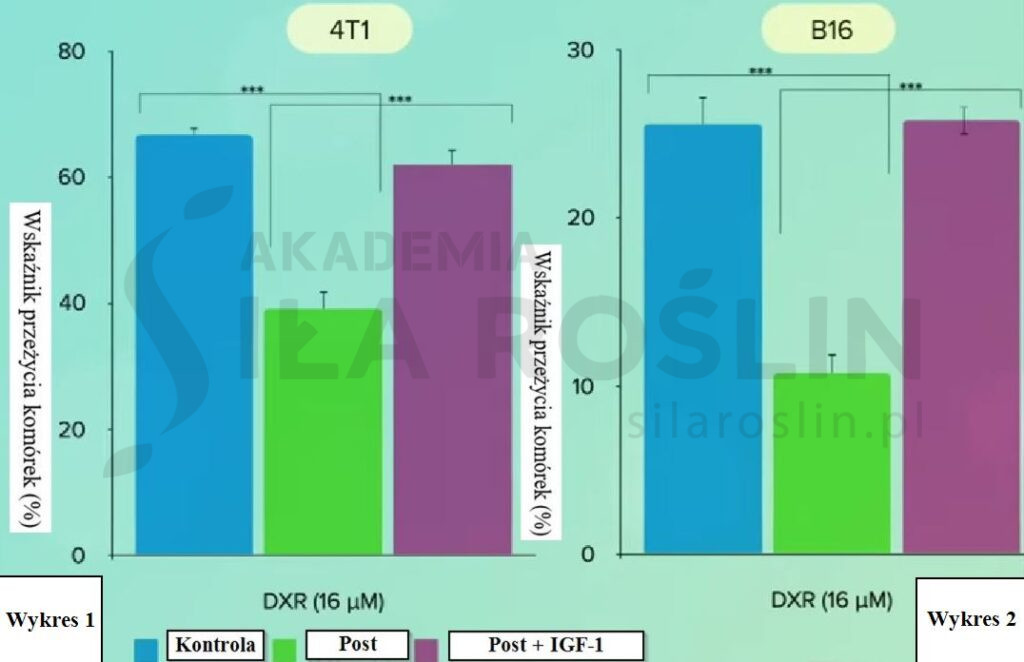
Sposób działania postu opiera się na obniżaniu poziomu hormonu stymulującego wzrost nowotworów, znanego jako insulinopodobny czynnik wzrostu 1 (IGF-1) [12]. To właśnie niższe stężenie IGF-1 odpowiada za różnice w odpowiedzi na post między komórkami zdrowymi i nowotworowymi [13]. W efekcie poprawia się zdolność chemioterapii do zabijania komórek rakowych, przy jednoczesnej ochronie komórek zdrowych [13]. Skąd o tym wiemy? Ponieważ w wyniku przywrócenia poziomu IGF-1 do poziomu sprzed postu całe to ochronne działanie zostaje zneutralizowane [13]. Poniższe wykresy (Wykres 1 i 2) [14] przedstawiają wzrost dwóch linii komórek nowotworowych, raka piersi (4T1) i czerniaka (B16). Jak widzimy, po zastosowaniu chemioterapii wskaźnik przeżycia komórek spadł odpowiednio do mniej więcej 60% i 20% [14]. Jeszcze lepsze efekty uzyskano, gdy te same komórki, przed wystawieniem na działanie leku, poddane zostały głodówce [14]. Wystarczyło jednak dodać trochę IGF-1 i nagle, przy tej samej dawce chemioterapii, wskaźnik przeżycia komórek z powrotem wzrasta, jakby postu nigdy nie było [14].
Korzyści z hamowania sygnalizacji IGF-1 mogą być zatem podwójne: ochrona tkanek zdrowych, przy jednoczesnym hamowaniu progresji nowotworu [12]. Co więcej, niewykluczone, że jest to również sposób, by do rozwoju raka w ogóle nie dopuścić [15]. Jak wyjaśniliśmy w artykule pt. „Jak nie umrzeć na raka”, obniżyć poziom IGF-1 można nie tylko przy zastosowaniu postu [16]. To prawda, w wyniku kilku dni głodówki stężenie IGF-1 spaść może o połowę [16], ale jest to w dużej mierze zasługa eliminacji spożycia białka [17]. Białko stanowi kluczowy czynnik determinujący stężenie krążącego IGF-1 w organizmie człowieka [17]. Oznacza to, że obniżenie spożycia białka, a szczególnie białka odzwierzęcego, może stać się istotnym elementem interwencji żywieniowych ukierunkowanych na profilaktykę nowotworów i starzenia się organizmu [17].
W badaniu z 2008 r. [17] pod względem poziomu IGF-1 porównano osoby na diecie w 100% roślinnej, o podaży białka zgodnej z ogólnymi zaleceniami (0,8 grama na kilogram masy ciała), oraz osoby na niskokalorycznej diecie tradycyjnej, które białka jadły mniej więcej tyle samo co przeciętny Amerykanin. Jak się okazało, w wyniku restrykcji kalorycznej w poziomie IGF-1 wszystkożerców odnotowano niewielki spadek [17]. Lepsze efekty zaobserwowano jednak wśród wegan [17]. Wygląda więc na to, że dieta oparta na nieprzetworzonych produktach roślinnych może nie tylko zmniejszać aktywność IGF-1, potencjalnie spowalniając tym samym proces starzenia się organizmu [18], ale i aktywować geny hamujące starzenie się organizmu do walki z rakiem [19].
Źródło: nutritionfacts.org
[1] Scrable H. Impersonalized medicine. Sci Transl Med. 2012;4(124):124ps6.[2] de Groot S, Pijl H, van der Hoeven JJM, Kroep JR. Effects of short-term fasting on cancer treatment. J Exp Clin Cancer Res. 2019;38(1):209.
[3] Sun L, Li Y-J, Yang X, Gao L, Yi C. Effect of fasting therapy in chemotherapy-protection and tumor-suppression: a systematic review. Transl Cancer Res. 2017;6(2):354-65.
[4] Caccialanza R, Cereda E, De Lorenzo F, Farina G, Pedrazzoli P, AIOM-SINPE-FAVO Working Group. To fast, or not to fast before chemotherapy, that is the question. BMC Cancer. 2018;18(1):337.
[5] Safdie FM, Dorff T, Quinn D, et al. Fasting and cancer treatment in humans: a case series report. Aging (Albany NY). 2009;1(12):988-1007.
[6] Haines I. The war on cancer: time for a new terminology. Lancet. 2014;383(9932):1883.
[7] Caccialanza R, Aprile G, Cereda E, Pedrazzoli P. Fasting in oncology: a word of caution. Nat Rev Cancer. 2019;19(3):177.
[8] Arends J, Bachmann P, Baracos V, et al. ESPEN guidelines on nutrition in cancer patients. Clin Nutr. 2017;36(1):11-48.
[9] Nencioni A, Caffa I, Cortellino S, Longo VD. Reply to 'Fasting in oncology: a word of caution’. Nat Rev Cancer. 2019 Mar;19(3):178. doi: 10.1038/s41568-018-0100-x. PMID: 30651605.
[10] Nencioni A, Caffa I, Cortellino S, Longo VD. Fasting and cancer: molecular mechanisms and clinical application. Nat Rev Cancer. 2018;18(11):707-19.
[11] Di Biase S, Longo VD. Fasting-induced differential stress sensitization in cancer treatment. Mol Cell Oncol. 2016;3(3):e1117701.
[12] Lee C, Longo VD. Fasting vs dietary restriction in cellular protection and cancer treatment: from model organisms to patients. Oncogene. 2011;30(30):3305-3316.
[13] Lee C, Safdie FM, Raffaghello L, et al. Reduced levels of IGF-I mediate differential protection of normal and cancer cells in response to fasting and improve chemotherapeutic index. Cancer Res. 2010;70(4):1564-72.
[14] Lee C, Raffaghello L, Brandhorst S, et al. Fasting cycles retard growth of tumors and sensitize a range of cancer cell types to chemotherapy. Sci Transl Med. 2012;4(124):124ra27.
[15] Longo VD, Mattson MP. Fasting: molecular mechanisms and clinical applications. Cell Metab. 2014;19(2):181-92.
[16] Thissen JP, Ketelslegers JM, Underwood LE. Nutritional regulation of the insulin-like growth factors. Endocr Rev. 1994;15(1):80-101.
[17] Fontana L, Weiss EP, Villareal DT, Klein S, Holloszy JO. Long-term effects of calorie or protein restriction on serum IGF-1 and IGFBP-3 concentration in humans. Aging Cell. 2008;7(5):681-7.
[18] McCarty MF. A low-fat, whole-food vegan diet, as well as other strategies that down-regulate IGF-I activity, may slow the human aging process. Med Hypotheses. 2003;60(6):784-92.
[19] Longo VD, Lieber MR, Vijg J. Turning anti-ageing genes against cancer. Nat Rev Mol Cell Biol. 2008;9(11):903-10.