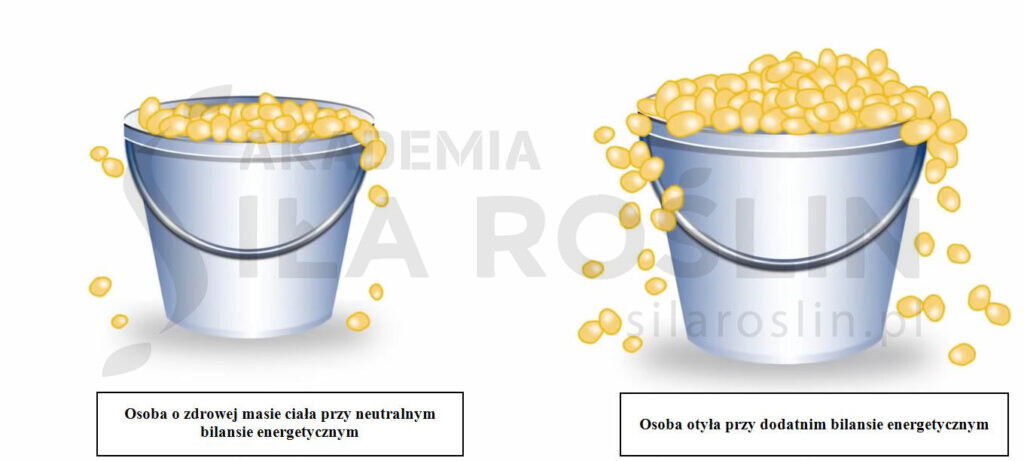
Efekt „rozlewania się” tłuszczu jako czynnik łączący otyłość z cukrzycą
Wolne kwasy tłuszczowe, czyli takie, które krążą w krwiobiegu w postaci „wolnej”, nie jako składnik trójglicerydów, prowadzą do rozwoju stanu zapalnego, powstania szkodliwych produktów rozkładu tłuszczu i wystąpienia stresu oksydacyjnego [1]. W efekcie dojść może do zaburzeń procesów sygnalizujących przyłączenie insuliny do receptora insulinowego, co prowadzi do rozwoju insulinooporności w mięśniach [1]. Insulinooporność, natomiast, jest przyczyną stanu przedcukrzycowego i cukrzycy typu 2. [1]
Wraz ze wzrostem poziomu tłuszczu we krwi zdolność organizmu do eliminowania z krwiobiegu cukru ulega osłabieniu [2]. Skąd pochodzi tłuszcz, który sieje całe to spustoszenie? Z naszego jedzenia i z naszej tkanki tłuszczowej.
U dorosłego człowieka liczba komórek tłuszczowych jest stała [3]. Co ciekawe odkrycia tego dokonano poprzez zmierzenie ilości radioaktywnego węgla w ludzkim DNA, skumulowanego w następstwie prób jądrowych [3]. W każdym razie, kiedy chudniemy nasze komórki tłuszczowe się kurczą, ponieważ pozbywają się tłuszczu, ale ich liczba pozostaje niezmieniona [3]. W odwrotnym przypadku, gdy przybieramy na wadze, nasze komórki tłuszczowe się rozciągają, ponieważ muszą pomieścić w sobie większe ilości tłuszczu [3]. Zatem większy brzuch, pupa, czy uda nie oznacza wcale większej liczby komórek tłuszczowych, tylko więcej tłuszczu w komórkach już istniejących. W pewnym momencie nasze komórki stają się na tyle przepełnione, że zgromadzony w nich tłuszcz zaczyna wylewać się z powrotem do krwiobiegu.
Poniższa ilustracja [4] przedstawia tzw. efekt „rozlewania się” tłuszczu (ang. spillover effect). Osoby otyłe nie tylko mają więcej tkanki tłuszczowej, ale w dodatku tłuszcz z ich komórek tłuszczowych nieustannie wylewa się do krwiobiegu [4]. Możliwe, że na tym właśnie polega związek między otyłością i cukrzycą [5]. Tłuszcz wylewa się z komórek tłuszczowych, gromadzi się w komórkach mięśniowych i wywołuje insulinooporność, która prowadzić może do rozwoju cukrzycy typu 2. [5]
Tłuszcz do krwiobiegu dostać się może również za pośrednictwem jamy ustnej. W badaniu z 2001 r. [6] porównano dietę niskowęglowodanową i niskotłuszczową. Zaobserwowano, że wśród uczestników na diecie niskowęglowodanowej tłuszcz zgromadził się w mięśniach w ciągu zaledwie dwóch godzin; tym samym wśród badanych w tej grupie obniżeniu uległa wrażliwość na insulinę [6]. Im wyższy poziom tłuszczu we krwi, tym słabsza staje się zdolność organizmu do usuwania cukru z krwiobiegu. Nie jest to wcale proces wieloletni, wystarczy zaledwie kilka godzin, by tłusty posiłek zaczął zaburzać odpowiednie wykorzystanie insuliny [6]. Dieta wysokotłuszczowa może zwiększać poziom tłuszczu we krwi; wzrostowi temu towarzyszy spadek wrażliwości insulinę [6].
Badania [2] pokazują wyraźnie, że tłuszcz we krwi hamuje transport glukozy i odpowiednie jej wykorzystanie w mięśniach. A przecież ok. 85% cukru z krwiobiegu pobierać powinny właśnie mięśnie. Zależność ta wskazuje również na istotną rolę, jaką w rozwoju insuliooporności odgrywa żywienie, a konkretnie wysokie spożycie tłuszczu [2].
Normalne stężenie wolnych kwasów tłuszczowych w krwiobiegu wynosi 10-50 mikromoli [2]. Wiemy już, że u osób otyłych tłuszcz z komórek tłuszczowych nieustannie wylewa się do krwiobiegu. Jednak problem wysokiego poziomu tłuszczu we krwi dotykać może nawet osób szczupłych [2]. Wszystko zależy tutaj od diety. Osoba o normalnej masie ciała spożywająca duże ilości tłuszczu może mieć taki sam poziom tłuszczu we krwi, co osoba otyła [2]. Na tej samej zasadzie otyłość w skutkach jest równie szkodliwa, co objadanie się całymi dniami masłem i bekonem, ponieważ u osób otyłych tłuszcz nieustannie wylewa się do krwiobiegu, niezależnie od ich sposobu odżywiania.
Źródło: https://nutritionfacts.org/
[1] J Ye. Role of insulin in the pathogenesis of free fatty acid-induced insulin resistance in skeletal muscle. Endocr Metab Immune Disord Drug Targets. 2007 Mar;7(1):65-74.[2] M Roden. How free fatty acids inhibit glucose utilization in human skeletal muscle. News Physiol Sci. 2004 Jun;19:92-6.
[3] K L Spalding, E Arner, P O Westermark, S Bernard, B A Bucholz, O Bergmann, L Blomgvist, J Hoffstedt, E Naslund, T Britton, H Concha, M Hassan, M Ryden, J Frisen, P Arner. Dynamics of fat cell turnover in humans. Nature. 2008 Jun 5;453(7196):783-7.
[4] S Hocking, D Samocha-Bonet, K L Milner, J R Greenfield, D J Chisholm. Adiposity and Insulin Resistance in Humans: The Role of the Different Tissue and Cellular Lipid Depots. Endocr Rev. 2013 Aug;34(4):463-500.
[5] J S Pankow, B B Duncan, M I Schmidt, C M Ballantyne, D J Couper, R C Hoogeveen, S H Golden: Athersclerosis Risk in Communities Study. Fasting plasma free fatty acids and risk of type 2 diabetes: the atherosclerosis risk in communities study. Diabetes Care. 2004 Jan;27(1):77-82.
[6] O P Bachmann, D B Dahl K Brechtel, J Machann, M Happ, T Maier, M Loviscach, M Stumvoll, C D Claussen, F Schick, H U Haring, S Jacob. Effects of intravenous and dietary lipid challenge on intramyocellular lipid content and the relation with insulin sensitivity in humans. Diabetes. 2001 Nov;50(11):2579-84.